В мире химии существует чрезвычайно обширная область исследований, которая посвящена изучению взаимодействия кислот и оснований. Это волнующее поле исследований предлагает нам увлекательное путешествие во внутренний мир реакций, обогащая наши знания о химических процессах и их значениях в нашей повседневной жизни. Одним из фундаментальных методов исследования является метод кислотно-основного титрования, при помощи которого мы можем получить глубокое понимание о взаимодействии кислот и оснований.
Концепция кислотно-основного титрования основана на том, что кислота и основание могут реагировать между собой, изменяя химическую структуру и свойства исходных веществ. Однако, вариативность их сочетания приводят к невозможности определения точного химического состава без дополнительного анализа. Именно поэтому метод кислотно-основного титрования становится наиболее эффективным способом изучения реакций кислот и оснований.
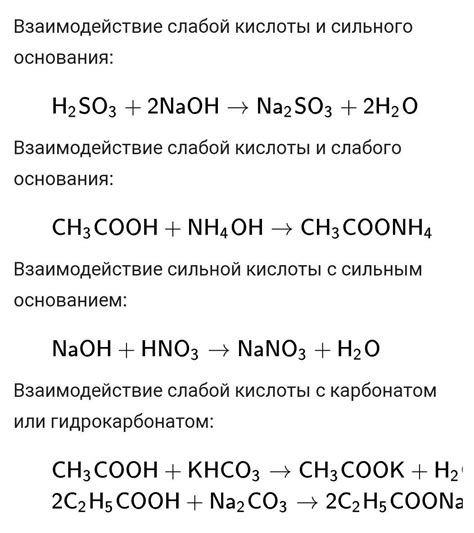
Ключевым принципом данного метода является реакция нейтрализации, которая происходит между кислотой и основанием. В результате этой реакции образуется вода и соль. Известно, что для каждой кислоты существует определенное основание, которое может нейтрализовать ее. Анализируя эту реакцию, мы можем вычислить точное количество основания, необходимое для полного нейтрализации кислоты.
Определение процесса нейтрализации кислот и щелочей
В данном разделе мы рассмотрим процесс, который позволяет определить точку эквивалентности при реакции кислоты и основы. Это важный метод анализа, в котором используются разные реактивы и инструменты для установления концентрации веществ.
- Проводится титрование – измерение количества добавленного реагента до наступления точки окончания реакции, которую иногда называют точкой перехода.
- Определение концентрации реагентов – расчет концентрации кислоты или основы с помощью известных данных о реакции.
- Выбор индикатора – это вещество, добавляемое в реакционную среду, чтобы показать изменение ее свойств, которое происходит в точке эквивалентности.
В процессе нейтрализации и титрования используются различные методы, такие как цветовой, электрохимический или компьютерный анализ для определения точки эквивалентности.
Определение метода кислотно основного титрования является важной частью химического анализа, помогающей установить концентрацию кислоты или основы в реакционной среде. Это необходимо для контроля качества промышленных продуктов, определения физиологических свойств различных веществ и выполнения других важных задач.
Историческое путешествие в мир развития техники нейтрализации веществ

| Период истории | Значимые открытия |
|---|---|
| Древний мир | Первые упоминания кислотных и щелочных веществ; экспериментальные наблюдения влияния их сочетания на окрашивание тканей и древесины; |
| Средние века | Арабские химики продвинались в изучении базовых принципов, включая простые методы титрования; Завершение развития идей Аль-Алканди о свойствах кислот; |
| Эпоха Просвещения | Открытие основных свойств кислых и щелочных соединений, отчетливое осознание различий между ними вплоть до идентификации их компонентов в XVIII-XIX веках. |
| XX век | Первое применение pH-метра для точного определения щелочности и кислотности раствора; разработка моделей и теорий, объясняющих процесс титрования. |
Применение метода кислотно-щелочного титрования было и остаётся одной из важнейших методик в различных областях, начиная от химического анализа и заканчивая проведением контроля качества продукции. Со временем развитие техники и науки способствовало улучшению метода, а новые открытия и инновации продолжают расширять его возможности, делая диагностику и исследования более точными и доступными.
Основные принципы проведения титрования

В данном разделе рассматриваются ключевые принципы, на которых основывается процесс проведения титрования с использованием кислот и основ. Титрование представляет собой экспериментальный метод, позволяющий определить концентрацию одного вещества через реакцию с другим веществом. Для успешного проведения титрования необходимо соблюдать следующие принципы: точность измерений, выбор правильных индикаторов, поддержание необходимых условий, а также обработка полученных данных.
Важным аспектом является точность измерений, которая достигается с помощью использования качественных лабораторных приборов и тщательной подготовки растворов. Кроме того, выбор правильных индикаторов играет решающую роль в определении конечной точки титрования. Индикатор - это вещество, изменяющее свой цвет при определенном изменении рН-среды. Использование подходящего индикатора позволяет определить конечную точку титрования с высокой точностью и надежностью.
Не менее важным фактором является поддержание необходимых условий во время проведения титрования, таких как температура и скорость перемешивания. Условия влияют на скорость протекания реакции и, следовательно, на точность определения концентрации исследуемого вещества.
Расчет значения pH раствора на основе полученных результатов титрования

Основной метод расчета pH раствора основан на обработке данных эксперимента с использованием уравнения нейтральности реакции титрования. Для этого необходимо знать концентрацию используемого раствора титранта, его стехиометрию и полученные значения объема и концентрации раствора титрата. Используя эти данные, можно рассчитать количество обратимо протекающих реакций и поместить полученные значения в уравнение нейтральности.
| Символ | Обозначение | Описание |
|---|---|---|
| c | Концентрация | Количество вещества, содержащегося в единице объема раствора |
| n | Стехиометрический коэффициент | Количество молей реагирующих веществ, участвующих в реакции |
| V | Объем | Данные об объеме раствора титранта |
В результате расчета получается значение концентрации водородных ионов (H+) в растворе, которые определяют кислотность или щелочность данного раствора. Это значение можно выразить через логарифмическую функцию, известную как pH. Чем ниже значение pH, тем больше кислотность раствора, а чем выше - тем больше щелочность.
Использование показателей для определения точки эквивалентности титрования

Определение эквивалентной точки титрования является важным этапом в процессе анализа. Для ее определения применяются различные типы показателей, которые меняют свой цвет или свойства в зависимости от pH среды. Эти изменения помогают определить точное значение эквивалентной точки титрования путем визуального наблюдения.
| Тип показателя | Принцип работы | Пример |
|---|---|---|
| Индикаторы кислотно-основного титрования | Меняют цвет в зависимости от pH среды | Фенолфталеин, метилоранж |
| Индикаторы окислительно-восстановительного титрования | Меняют цвет в зависимости от окислительно-восстановительного потенциала | Дипероксид метиленовый синий |
Для каждого типа титрования применяются подходящие показатели. Выбор показателя зависит от pH среды и ожидаемого изменения состояния вещества при прохождении эквивалентной точки титрования. Например, фенолфталеин обращает свой цвет с безцветного в присутствии кислоты к насыщенно-розовому в присутствии щелочи.
Использование показателей является одним из основных методов для определения эквивалентной точки титрования. Этот метод позволяет получить визуальное подтверждение достижения точки эквивалентности и улучшить точность результатов анализа.
Виды титрования на основе реакций кислот и оснований
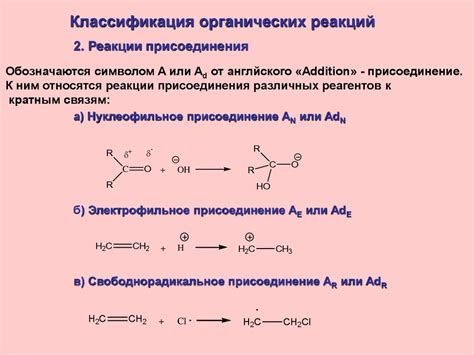
- Нейтрализационное титрование: при этом виде титрования кислота и основание реагируют между собой, образуя воду и соль. Реакция происходит до точки эквивалентности, когда количество добавленного титранта полностью реагирует с реагентом в пробе. Точка эквивалентности обозначается изменением индикатора, что позволяет точно определить конечное количество добавленного титранта.
- Окислительно-восстановительное титрование: это вид титрования, основанный на взаимодействии окислителя и восстановителя. При реакции окисления одного реагента и восстановления другого происходит перенос электронов. Реакция продолжается до точки эквивалентности, которая определяется изменением цвета индикатора.
- Комплексометрическое титрование: в этом виде титрования основой является реакция образования или растворения комплексов. Комплексообразующие вещества (чаще всего лиганды) взаимодействуют с ионами металла, образуя стабильные соединения. Реакция продолжается до точки эквивалентности, когда все ионы металла образуют комплексы или все комплексы растворяются.
Роль и перспективы применения метода кислотно-основного титрования в практических задачах

Метод кислотно-основного титрования нашел свое применение в медицине, позволяя определять концентрацию различных веществ в биологических средах, таких как кровь или моча. Это важное средство диагностики, позволяющее выявить наличие или отсутствие определенных веществ, а также отследить их концентрацию в организме. Кроме того, метод кислотно-основного титрования находит применение в пищевой промышленности, где его используют для определения концентрации различных веществ в пищевых продуктах. Такой анализ помогает обеспечить качество и безопасность пищевых продуктов, контролировать процессы производства и расчет дозировки нужных компонентов для достижения определенных вкусовых характеристик и сохранения полезных свойств.
- Одной из областей, где этот метод нашел свое практическое применение, является анализ почв и воды. Определение содержания кислот и основ в почвах позволяет судить о качестве почвенного покрова, его способности удерживать важные макро- и микроэлементы, а также влиять на питательные свойства почвы. Анализ воды с использованием метода кислотно-основного титрования позволяет определить ее качество, выявить загрязнения и контролировать содержание различных веществ, таких как минеральные соли или тяжелые металлы.
- В химической промышленности метод кислотно-основного титрования применяется для определения концентрации различных веществ, которые играют ключевую роль в процессах химического синтеза или контроля качества готовой продукции. Такой анализ позволяет достичь требуемой степени чистоты продукта, а также обеспечить его соответствие установленным стандартам и нормам безопасности.
Таким образом, метод кислотно-основного титрования является универсальным инструментом, используемым в различных сферах науки и промышленности. Его применение позволяет определить концентрацию кислот и основ с высокой точностью, что имеет важное значение для множества практических задач и достижения поставленных целей. Непрерывное развитие этого метода и его технических аспектов открывает новые перспективы для его применения в будущем.
Преимущества и ограничения метода титрования кислот и оснований

Преимущества:
- Высокая точность и повторяемость результатов. Метод титрования обладает очень высокой точностью измерений, что позволяет получить достоверную информацию о содержании кислот и оснований в растворе.
- Простота и удобство проведения. Титрование является относительно простым и доступным методом, который может быть проведен с минимальными затратами времени и ресурсов.
- Возможность использования в широком диапазоне областей применения. Титрование может быть использовано в различных отраслях науки и промышленности для контроля качества продукции, медицинских и фармацевтических исследований и других сфер.
Ограничения:
- Необходимость калибровки индикаторов. Для достижения наибольшей точности, требуется калибровка используемых индикаторов, что может занимать время и быть трудоемким процессом.
- Существующие ограничения в выборе реагентов. В некоторых случаях, выбор реагентов для титрования может быть ограничен, что может затруднить проведение исследований или анализов.
- Необходимость применения определенных условий и ограничений. В ходе титрования периодически требуется соблюдение определенных условий (температура, pH и т. д.), что может повлиять на получение точных результатов.
Вопрос-ответ

Какой метод используется в кислотно-основном титровании?
В кислотно-основном титровании используется метод определения концентрации раствора кислоты или основы с помощью титрования, при котором мера объема раствора титранта точно вступает в реакцию с исследуемым раствором.
Каким образом определяется концентрация кислоты или основы при кислотно-основном титровании?
Концентрация кислоты или основы определяется путем измерения объема титранта (раствора с известной концентрацией) необходимого для полного их нейтрализации. Важно учитывать эквивалентность реагирующих веществ и использовать индикаторы, позволяющие определить момент полной нейтрализации.