Когда мы говорим о таблице Менделеева, мы обращаемся к основному инструменту, который позволяет нам понять устройство и взаимодействие химических элементов. Эта таблица, по сути, отражает гигантский и разнообразный мир атомов и молекул, и легко увидеть, почему порядковый номер каждого элемента играет невероятно важную роль.
Безусловно, в таблице Менделеева нет случайных или бессмысленных элементов. Все упорядочено и систематизировано таким образом, чтобы создать основу для понимания химии и ее связей с другими науками. Поэтому, порядковый номер каждого элемента, выраженный числом, не является просто эстетическим декором или удобным средством для организации таблицы - он содержит самую суть и глубинное значение.
Понимая и учитывая порядковый номер в таблице Менделеева, мы можем лучше воспринять фундаментальные законы химии и предсказать свойства и реактивность различных элементов. Каждый порядковый номер дает нам уникальную информацию о структуре, электронной конфигурации, атомных и физических свойствах элементов. Использование порядкового номера позволяет нам заполнить пробелы в нашем понимании химических закономерностей и создать основу для дальнейшего исследования и развития науки.
Основные принципы, определяющие значение последовательного числа в упорядоченной справочной таблице Менделеева
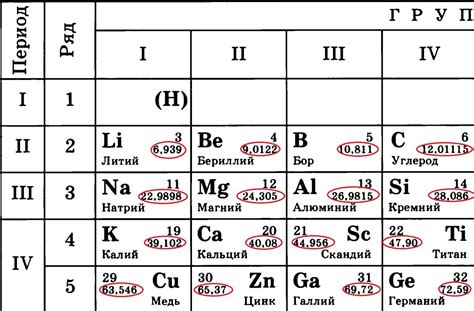
Принцип установления последовательного числа основан на систематическом подходе к классификации химических элементов. Он предполагает постепенное увеличение числа с каждым последующим элементом, отражая изменение электронной конфигурации в атоме.
С помощью последовательных чисел в таблице Менделеева мы можем определить, какие элементы будут располагаться рядом с друг другом, образуя группы и периоды. Группы элементов с одинаковым последовательным числом обладают аналогичными химическими свойствами, что делает эту систему классификации справочной таблицы исключительно полезной и удобной для химиков и научных исследований.
- Множество синонимов понятия "порядковый номер":
- Учетный номер
- Ранговый номер
- Систематический номер
- Последовательный номер
Уникальный аспект упорядоченности элементов в таблице как важного аспекта их изучения и практического применения

Систематическая организация элементов в таблице Менделеева отражает их внутреннюю структуру и связи между ними. Каждый порядковый номер в таблице отмечает уникальное положение элемента и служит для определения его физических и химических свойств.
Упорядоченность элементов в таблице позволяет устанавливать закономерности и тренды, которые полезны для прогнозирования свойств новых элементов или неизвестных соединений. Кроме того, она упрощает поиск и анализ информации о конкретном элементе и его взаимодействиях с другими веществами.
Другой важный аспект упорядоченности элементов в таблице Менделеева заключается в возможности классификации химических реакций и процессов. Знание порядкового номера элемента позволяет определить его место в таблице и, следовательно, предсказать его химическое поведение в различных условиях.
В итоге, понимание и использование упорядоченности элементов в таблице Менделеева является неотъемлемой частью химического образования и исследований. Это позволяет ученым и инженерам разрабатывать новые материалы, оптимизировать процессы и создавать инновационные решения для различных областей науки и промышленности.
Определение положения элемента в таблице Менделеева
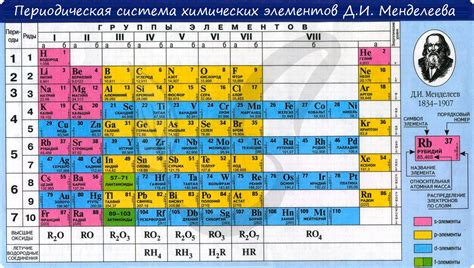
Порядковый номер элемента отражает его положение в возрастающей последовательности и связан с количеством протонов в атомном ядре атома данного элемента. В таблице Менделеева каждый горизонтальный ряд, называемый периодом, представляет атомы с одинаковым количеством электронных оболочек, а каждая вертикальная группа, называемая группой или семейством, обозначает элементы с одинаковым количеством внешних электронов.
Порядковый номер элемента также отражает его относительную массу, которая является суммой протонов и нейтронов в атоме. Благодаря этому, элементы с близкими порядковыми номерами обычно имеют схожие химические свойства и образуют подобные соединения.
Связь между электронной структурой элементов и их положением в таблице
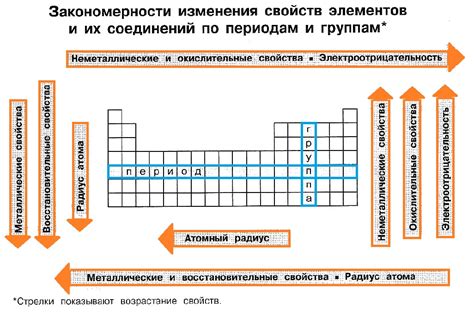
В данном разделе мы рассмотрим взаимосвязь между строением электронных оболочек элементов и их местом в периодической системе химических элементов. Все химические элементы имеют уникальное расположение в таблице Менделеева, которое определяется их электронной структурой. Понимание этой связи позволяет установить закономерности между свойствами элементов и предсказывать их химическое поведение.
Также, важным фактором является положение элементов в периодической системе. Оно определяет их относительное положение по прошествии периодов и групп. Элементы в одной группе имеют аналогичное число электронов во внешней оболочке, что делает их более схожими по свойствам. При этом, по мере увеличения порядкового номера, электронные оболочки элементов становятся все более заполненными, что влияет на их реакционную способность и химическую активность.
Исследования связи между электронной структурой и положением элементов в таблице Менделеева позволяют лучше понять и объяснить все многообразие свойств химических элементов. Обладая этим знанием, ученые могут прогнозировать химическое поведение новых элементов и создавать новые соединения с требуемыми свойствами.
Закономерности в периодической таблице Менделеева
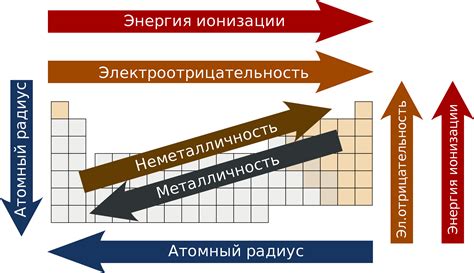
Первая закономерность, которую можно обнаружить в таблице Менделеева, - это периодичность химических свойств элементов. Путем анализа вертикальных (групп) и горизонтальных (периодов) рядов элементов можно увидеть регулярность в повторении химических характеристик. Например, элементы в одной группе обычно имеют схожие свойства, такие как одинаковая валентность и способность образовывать схожие химические соединения. С другой стороны, элементы в одном периоде имеют аналогичные электронные конфигурации.
Вторая закономерность, отмечаемая в таблице Менделеева, - это постепенное изменение свойств элементов отлагандлевской серии к усложненным элементам. Это означает, что при движении по периоду свойства элементов постепенно меняются, становясь более разнообразными и сложными. Например, при переходе от легких элементов, таких как литий и бериллий, к более тяжелым элементам, таким как углерод и кислород, мы наблюдаем появление новых свойств, таких как возможность образования двойных или тройных связей и способность кислорода к образованию оксидов.
Третья закономерность, которую можно найти в таблице Менделеева, - это группировка элементов по типу атомов и электронной конфигурации. В таблице Менделеева есть блоки, состоящие из элементов, имеющих схожие электронные оболочки и атомные структуры. Например, элементы из блока p обладают уровнями энергии, заполненными p-электронами, и обычно образуют оокиси, галогены или инертные газы.
Таким образом, периодическая таблица Менделеева представляет собой не только упорядоченный список элементов, но и отображает ряд закономерностей, важных для наглядного представления и анализа химических свойств и структуры элементов.
Химические свойства и реакции в контексте положения элементов в таблице элементов Д.И.Менделеева

Каждый элемент имеет уникальные электронные конфигурации, которые определяют его химические свойства и реактивность. В таблице Менделеева элементы расположены таким образом, чтобы элементы с похожей электронной конфигурацией находились в том же столбце, образуя группы. Группы элементов имеют сходные химические свойства и образуют реакции схожего типа. Например, элементы группы 1 (щелочные металлы) имеют одну внешнюю электрон в своей электронной оболочке, что делает их чрезвычайно реакционноспособными.
Положение элемента в периоде также влияет на его химические свойства и реактивность. Каждый период начинается с щелочного металла и заканчивается инертным газом. Это означает, что свойства элементов в периоде изменяются по мере приближения к концу периода. Например, элементы в начале периода обладают металлическими свойствами и склонностью к окислению, в то время как элементы в конце периода обладают неметаллическими свойствами и малой реакционностью.
Таким образом, положение элемента в таблице Менделеева и его порядковый номер отражают его химические свойства и способность к участию в химических реакциях. Это позволяет ученым предсказывать химические свойства и взаимодействия элементов и использовать эту информацию в различных областях химии и материаловедения.
Значимость порядкового числа в периодической системе для предсказания и открытия новых веществ

В периодической системе химических элементов порядковое число каждого элемента играет фундаментальную роль, позволяя уникально идентифицировать и классифицировать вещества. Однако, помимо своей классификационной функции, порядковое число также обладает важной объяснительной способностью, что дает возможность предсказывать и открывать новые вещества.
Порядковое число элемента в периодической системе определяет его положение в таблице, а также характеризует количество протонов в атомном ядре элемента. Между количеством протонов и химическими свойствами элемента существует тесная связь, что объясняет сходство и различия между разными элементами. Благодаря этой связи ученые могут предсказать химические свойства новых, еще не открытых элементов.
- Прогнозирование химических свойств элементов позволяет определить их возможные соединения и реакции, что открывает перспективы в синтезе новых веществ с желаемыми свойствами. Например, предсказание химического поведения сталкивающихся элементов может помочь в разработке эффективных катализаторов.
- Кроме того, порядковое число также помогает ученым выявлять закономерности в свойствах элементов, основанные на их расположении в таблице Менделеева. Это позволяет заполнять пробелы в периодической системе, открывая новые элементы и прогнозируя их свойства.
- Порядковое число стимулирует интерес к исследованию и поиску новых веществ с помощью синтеза и анализа, ведь оно демонстрирует возможность открытия неизведанных ранее химических элементов и соединений.
Таким образом, порядковое число в периодической системе Менделеева не только структурирует знания о химических элементах, но и является мощным инструментом для предсказания и открытия новых веществ. Оно открывает перед учеными огромную перспективу в области развития материалов и технологий, позволяя преодолеть границы существующих знаний и расширить возможности человечества в области химии и природных наук.
Вопрос-ответ

Каково значение порядкового номера в таблице Менделеева?
Порядковый номер в таблице Менделеева указывает на количество протонов в атомном ядре атома химического элемента.
Зачем нужен порядковый номер в таблице Менделеева?
Порядковый номер помогает упорядочить химические элементы и определить их свойства, а также предсказать их поведение в химических реакциях.
Какие элементы имеют наибольшие порядковые номера?
Самые большие порядковые номера в таблице Менделеева у трансурановых элементов, таких как уран, плутоний и америций, которые имеют порядковые номера свыше 92.
Что происходит с химическими свойствами элементов при изменении порядкового номера?
С изменением порядкового номера меняются и химические свойства элементов. Например, с увеличением порядкового номера уменьшается электроотрицательность элементов, а также возрастает их радиус и масса атомов.
Какие закономерности можно обнаружить, изучая порядковые номера в таблице Менделеева?
Изучая порядковые номера в таблице Менделеева, можно обнаружить периодические закономерности, такие как изменение радиуса атомов, электроотрицательности, валентности и многих других свойств вдоль периодов и групп химических элементов.
Каково значение порядкового номера в таблице Менделеева?
Значение порядкового номера в таблице Менделеева - это уникальный номер, присвоенный каждому химическому элементу в соответствии с их атомным номером. Этот номер указывает на количество протонов в ядре атома и определяет его положение в периодической системе элементов. Чем больше порядковый номер, тем больше атомные масса и энергия элемента.